Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Phần trắc nghiệm (7 điểm) SVIP
Yêu cầu đăng nhập!
Bạn chưa đăng nhập. Hãy đăng nhập để làm bài thi tại đây!
Trong hợp chất Na2SO4, số oxi hóa của sulfur là
Xét phản ứng sau:
3HCl + HNO3 → Cl2 + NOCl + 2H2O
Chất khử trong phản ứng trên là
Cho phản ứng chuẩn độ muối Mohr (FeSO4.(NH4)2SO4.6H2O) trong môi trường acid:
Cr2O72− + 14H+ + 6Fe2+→2Cr3+ + 6Fe3+ + 7H2O
Cần bao nhiêu milimol potassium dichromate để oxi hóa 24 cm3 dung dịch muối Mohr 0,5 M trong môi trường acid (làm tròn kết quả đến chữ số hàng đơn vị)?
Trả lời: .
Quá trình hình thành nitrogen dioxide gồm 2 bước:
Bước 1: N2 + O2 → 2NO
Bước 2: 2NO + O2 → 2NO2
Phản ứng tổng thể: N2 + 2O2 → 2NO2
Biết biến thiên enthalpy của phản ứng tổng thể là +68 kJ/mol.
(Nhấp vào ô màu vàng để chọn đúng / sai)| a) Phản ứng tổng thể tỏa nhiệt ra môi trường. |
|
| b) Cả hai bước đều là phản ứng tỏa nhiệt. |
|
| c) Cả hai bước đều là phản ứng thu nhiệt. |
|
| d) Phản ứng tổng thể diễn ra không thuận lợi ở điều kiện thường. |
|
Phản ứng giữa ethane và chlorine tạo ra ethyl chloride và khí hydrogen chloride là phản ứng tỏa nhiệt. Phương trình phản ứng:
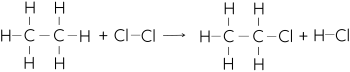
Cho biết năng lượng của một số liên kết như sau:
Liên kết | Năng lượng liên kết (kJ/mol) |
C-Cl | +340 |
C-C | +350 |
C-H | +410 |
Cl-Cl | +240 |
H-Cl | +430 |
Biến thiên enthalpy chuẩn của phản ứng trên là bao nhiêu kJ/mol (làm tròn kết quả đến chữ số hàng đơn vị)?
Trả lời: .
Khi các phản ứng dưới đây được thực hiện trong một buồng kín, phản ứng nào sẽ làm nhiệt độ trong buồng tăng lên?
Thực hiện 3 thí nghiệm như hình sau:
Thí nghiệm 1: Thả mẩu kẽm (2 gam) vào dung dịch HCl 1 M.
Thí nghiệm 2: Thả mẩu kẽm (2 gam) vào dung dịch HCl 0,5 M.
Thí nghiệm 3: Thả bột kẽm (2 gam) vào dung dịch HCl 1 M.

| a) Cả ba thí nghiệm trên đều có khí thoát ra. |
|
| b) Ống nghiệm 2 có tốc độ phản ứng nhanh hơn ống nghiệm 1 do ảnh hưởng của nồng độ HCl. |
|
| c) Tốc độ phản ứng trong ống nghiệm 3 là nhanh nhất do ảnh hưởng của diện tích tiếp xúc. |
|
| d) Nếu đun nóng cả 3 ống nghiệm thì tốc độ phản ứng xảy ra sẽ như nhau. |
|
Đơn vị nào sau đây không dùng để biểu diễn tốc độ phản ứng?
Xét phản ứng sau:
A+B→C+D
Tại thời điểm 4,5 phút sau khi phản ứng bắt đầu, nồng độ chất A đo được là 0,587 M và tốc độ phản ứng tại thời điểm đó là 2,1.10-2 mol/(L.min).
Giả sử tốc độ phản ứng không thay đổi đáng kể trong khoảng từ 4,5 - 6 phút. Nồng độ chất A đo được tại thời điểm 6 phút sau khi bắt đầu là bao nhiêu?
Trong tự nhiên, bromine thường gặp dưới dạng nào sau đây?
Trong quá trình điều tra vụ án, cảnh sát muốn làm rõ dấu vân tay của nghi phạm trên một bề mặt. Họ đã sử dụng một halogen có khả năng thăng hoa, khi đun nóng tạo ra hơi màu tím bám vào dấu vân tay. Halogen được sử dụng là
Cho dãy các halogen: Cl2, Br2, F2, I2 với các nhiệt độ sôi không tương ứng là -188,1 oC; -34,1 oC; 59,2 oC; 185,5 oC. Nhiệt độ sôi của Br2 là bao nhiêu oC?
Trả lời: .
Đốt cháy hoàn toàn một mẩu dây sắt trong khí chlorine dư. Sau phản ứng thu được 42,12 gam chất rắn màu nâu đỏ. Khối lượng của mẩu dây sắt ban đầu là
Trong các hợp chất halogen halide (HX) có chứa liên kết
Hòa tan 8,7 gam một mẫu quặng pyrolusite (chứa MnO2) vào dung dịch HCl dư, đun nóng. Dẫn toàn bộ khí chlorine sinh ra sau phản ứng vào dung dịch KI, thu được 11,92 gam muối KCl. Tính thành phần phần trăm của MnO2 trong mẫu quặng pyrolusite (làm tròn kết quả đến chữ số hàng đơn vị).
Trả lời: .
Ion halide nào có tính khử mạnh nhất?
Dùng thông tin sau để trả lời các câu 1 và câu 2: Tiến hành đo tốc độ phản ứng phân hủy N2O5 thu được kết quả trong bảng dưới đây.
2N2O5(g)→4NO2(g)+O2(g)

Biểu thức tốc độ phản ứng phân hủy N2O5 là
Tốc độ phản ứng phân hủy N2O5 trong 100 s đầu tiên là
