Cho 3 miếng Al vào 3 cốc đựng dd HNO3 có nồng độ khác nhau. Cốc 1 thấy có khí không màu bay ra và hoá nâu ngoài không khí. Cốc 2 thấy thoát ra khí không màu ko mùi, không cháy, nhẹ hơn oxi. Cốc 3 không thấy có khí nào bay ra, thu được dd trong suốt. a, Viết các PTHH b, Nếu lượng Al tan ra ở mỗi cốc là 5,4g thì lượng HNO3 dùng trong mỗi trường hợp là bao nhiêu mol. Tính thể tích khí thoát ra ở cốc 1 và cốc 2 (điều kiện tiêu chuẩn)
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Những câu hỏi liên quan

24 tháng 4 2019
Đáp án B
● Giả sử 2 chất tan đó là: Fe(NO3)3 và HNO3 dư.
⇒ nFe(NO3)3 = nHNO3 dư = x.
Bảo toàn electron ta có: 3nNO = 3nFe Û nNO = x.
+ Bảo toàn nguyên tố nito: ∑nHNO3 = 3nFe(NO3)3 + nHNO3 dư + nNO.
Û y = 3x + x + x Û y = 5x
● Giả sử 2 chất tan đó là Fe(NO3)3 và Fe(NO3)3.
⇒ nFe(NO3)3 = nFe(NO3)2 = x/2.
Bảo toàn electron ta có: nNO = (3nFe(NO3)3 + 2nFe(NO3)2) ÷ 3 = 5x/6
+ Ta có: ∑nHNO3 = 4nNO Û y = 10x/3

17 tháng 5 2019
Đáp án B
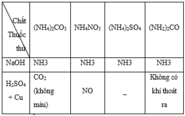
Nhận thấy trong các đáp án chỉ có NH4NO3 thỏa mãn.
Phương trình minh họa:
NaOH + NH4NO3 → H2O + NaNO3 + NH3
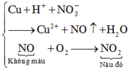

a) PTHH: \(Al+4HNO_3\rightarrow Al\left(NO_3\right)_3+NO\uparrow+2H_2O\) (1)
\(10Al+36HNO_3\rightarrow10Al\left(NO_3\right)_3+3N_2\uparrow+18H_2O\) (2)
\(8Al+30HNO_3\rightarrow8Al\left(NO_3\right)_3+3NH_4NO_3+9H_2O\) (3)
b) Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_{HNO_3\left(1\right)}=0,8\left(mol\right)\\n_{HNO_3\left(2\right)}=0,72\left(mol\right)\\n_{HNO_3\left(3\right)}=0,75\left(mol\right)\end{matrix}\right.\)
Mặt khác: \(\left\{{}\begin{matrix}n_{NO}=0,2\left(mol\right)\\n_{N_2}=0,06\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{NO}=0,2\cdot22,4=4,48\left(l\right)\\V_{N_2}=0,06\cdot22,4=1,344\left(l\right)\end{matrix}\right.\)