Đốt cháy hoàn toàn 12,88 gam hỗn hợp X gồm một axit no, đơn chức, mạch hở và một ancol no, đơn chức, mạch hở được 0,54 mol CO2 và 0,64 mol H2O. Thực hiện phản ứng este hóa hoàn toàn lượng hỗn hợp trên thì thu được m gam este. Giá trị của m là
A. 10,20 gam
B. 8,82 gam.
C. 12,30 gam
D. 11,08 gam


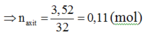

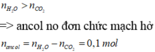
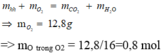
nancol = nH2O – nCO2 = 0,64 – 0,54 = 0,1
Bảo toàn khối lượng:
mX = mC + mH + mO → 12,88 = 0,54.12 + 0,64.2.1 + mO(X) → mO(X) = 5,12 g
nO(x) = 5,12/16 = 0,32 mol mol
nO(X) = nancol + 2naxit → 0,32 = 0,1 + 2naxit → naxit = 0,11 mol
Gọi x, y lần lượt là số nguyên tử C trong axit và ancol
0,11x + 0,1y = 0,54 → 11x + 10y = 54 → x = 4, y = 1
→ Công thức phân tử của axit và ancol lần lượt là: C3H7COOH và CH3OH
→ m = 0,1.102 = 10,2 gam
→ Đáp án A