1. Hòa tan 4,4g hỗn hợp A gồm Mg và Ca vào nước dư. Sau khi phản ứng xảy ra hoàn toàn, thu được m gam chất rắn và 1,12 lít khí hidro (đktc) a. Tính m b. Tính % khối lượng của từng kim loại trong hỗn hợp A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(a) m_{Cu} = 9,6(gam)\\ n_{Al} = a(mol) ; n_{Fe} = b(mol)\\ \Rightarrow 27a + 56b = 16,55 -9,6 =6,95(1)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = 1,5a + b = \dfrac{3,92}{22,4} = 0,175(2)\\ (1)(2) \Rightarrow a = 0,05 ; b = 0,1\\ m_{Al} = 0,05.27 = 1,35(gam); n_{Fe} = 0,1.56 = 5,6(gam)\)
\(b) n_{HCl} = 2n_{H_2} = 0,175.2 = 0,35(mol) \Rightarrow m_{HCl} = 0,35.36,5 = 12,775(gam)\)

a) PTHH: 2Al + 6 HCl -> 2 AlCl3 + 3 H2
x___________3x______________1,5x(mol)
Fe +2 HCl -> FeCl2 + H2
y___2y____y______y(mol)
b) Ta có: m(rắn)= mCu=0,4(g)
=> m(Al, Fe)=1,5-mCu=1,5-0,4=1,1(g)
nH2= 0,04(mol)
Ta lập hpt:
\(\left\{{}\begin{matrix}27x+56y=1,1\\1,5x+y=0,04\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,02\\y=0,01\end{matrix}\right.\)
=> mAl=27.0,02=0,54(g)
mFe=56.0,01=0,56(g)

\(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
____0,05<------------------------0,05
=> mFe = 0,05.56 = 2,8 (g)
=> mCu = 6 - 2,8 = 3,2 (g)
=> D

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1(mol)\\ a,Zn+2HCl\to ZnCl_2+H_2\\ b,n_{ZnCl_2}=0,1(mol)\\ \Rightarrow m_{ZnCl_2}=0,1.136=13,6(g)\\ c,n_{Zn}=0,1(mol)\\ \Rightarrow \%_{Zn}=\dfrac{0,1.65}{20}.100\%=32,5\%\\ \Rightarrow \%_{Ag}=100\%-32,5\%=67,5\%\)




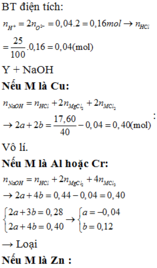

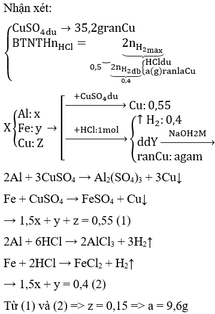
a) Chất rắn không tan là Mg
\(Ca + 2H_2O \to Ca(OH)_2 + H_2\\ n_{Ca} = n_{H_2} = \dfrac{1,12}{22,4} = 0,05(mol)\\ m = m_{Mg} = m_A - m_{Ca} = 4,4 - 0,05.40 = 2,4(gam)\\ b)\\ \%m_{Mg} = \dfrac{2,4}{4,4}.100\% = 54,55\%\\ \%m_{Ca} = 100\% - 54,55\%=45,45\%\)