Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Sự thay đổi số electron ở lớp ngoài cùng trong cùng 1 hàng khi đi từ trái sang phải:
+ Hàng thứ 1: Số electron ở lớp ngoài cùng tăng dần từ 1 đến 2
+ Hàng thứ 2: Số electron ở lớp ngoài cùng tăng dần từ 1 đến 8
+ Hàng thứ 3: Số electron ở lớp ngoài cùng tăng dần từ 1 đến 8

X có 8e -> X là Oxygen (O), có hóa trị II
Y có 17e -> Y là Chlorine (Cl), có hóa trị I
Z có 11e -> Z là Sodium (Na), có hóa trị I
a)
- X và Z:
CTHH là \(Na^I_xO_y^{II}\left(x,y\inℕ\right)\)
Theo quy tắc hóa trị: \(I\cdot x=II\cdot y\Leftrightarrow\dfrac{I}{II}=\dfrac{y}{x}\)
Thường thì ta lấy các số x và y đơn giản nhất, nên x = 2; y = 1.
Vậy CTHH là Na2O.
Tương tự, ta có:
- Y và Z: CTHH là NaCl;
- X với X: CTHH là O2
b) Kiểu liên kết hóa học giữa các nguyên tử trong các hợp trên là:
- X và Z: liên kết ion
- Y và Z: liên kết ion
- X với X: liên kết cộng hóa trị
c) Dự đoán 2 tính chất của hợp chất được tạo thành trong trường hợp X và Z; Y và Z: là chất rắn ở điều kiện thường, khó nóng chảy.

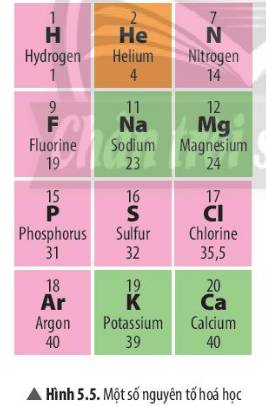
- Nguyên tử M có 2 electron ở lớp ngoài cùng => M nằm ở nhóm IIA
- Nguyên tử M có 3 lớp electron => M nằm ở chu kì 3
=> M thuộc ô số 12, nằm ở nhóm IIA, chu kì 3
- Ô số 12 màu xanh => Nguyên tử M là kim loại

- Thành phần chính của nước rửa tay khô là cồn ethanol: gồm 2 nguyên tử carbon, 6 nguyên tử hydrogen, 1 nguyên tử oxygen
=> Khối lượng phân tử của ethanol = 12 amu x 2 + 1 amu x 6 + 16 amu x 1 = 46 amu

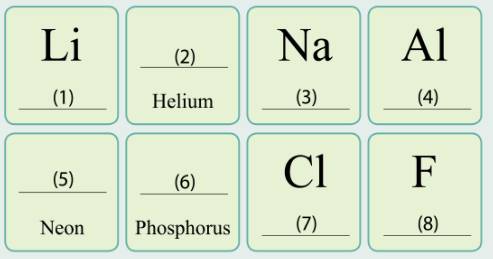
(1): Lithium
(2): He
(3): Sodium
(4): Aluminium
(5): Ne
(6): P
(7): Chlorine
(8): Fluorine

Số electron ở lớp ngoài cùng của nguyên tử Na =1
Số electron ở lớp ngoài cùng của ion Na+ =8
=>Số electron ở lớp ngoài cùng của ion Na+ nhiều hơn số electron ở lớp ngoài cùng của nguyên tử Na
Số electron ở lớp ngoài cùng của nguyên tử Cl =7
Số electron ở lớp ngoài cùng của ion Cl- =8
=>Số electron ở lớp ngoài cùng của ion Cl- nhiều hơn số electron ở lớp ngoài cùng của nguyên tử Cl
Số electron lớp ngoài cùng của `Na` bé hơn ion `Na^+`
Số electron lớp ngoài cùng của `Cl` bé hơn ion `Cl^-`

(1): Lithium
(2): He
(3): Natrium
(4): Aluminum
(5): Ne
(6): P
(7): Chlorine
(8): Fluorine

Bạn tham khảo nhé.
Để tính khối lượng nguyên tử của X, ta cần tìm khối lượng của 4 nguyên tử oxy trong phân tử và trừ đi khối lượng phân tử.
Theo đề bài, phân tử có 3 nguyên tử X và 4 nguyên tử oxy, do đó khối lượng phân tử là:
M = 3M(X) + 4M(O)
Với M(X) và M(O) lần lượt là khối lượng nguyên tử của nguyên tố X và oxy.
Ta biết khối lượng phân tử M là 232 amu, và khối lượng nguyên tử của oxy là khoảng 16 amu. Thay vào đó, ta có:
232 amu = 3M(X) + 4(16 amu) 232 amu = 3M(X) + 64 amu 3M(X) = 168 amu M(X) = 56 amu
Vậy khối lượng nguyên tử của nguyên tố X là 56 amu.
Từ kết quả trên, ta có thể xác định tên và ký hiệu hóa học của nguyên tố X bằng cách tham khảo bảng tuần hoàn các nguyên tố hóa học. Theo bảng tuần hoàn, nguyên tố có khối lượng nguyên tử gần nhất với 56 amu là Ba (Barium). Vì vậy, nguyên tố X có thể là Barium (Ba)
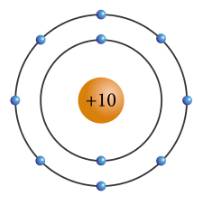
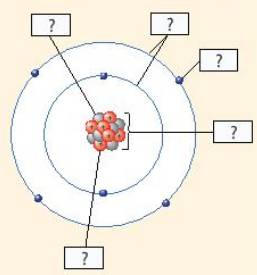
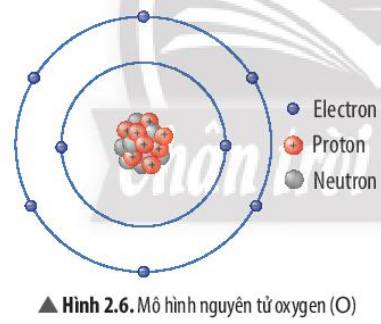
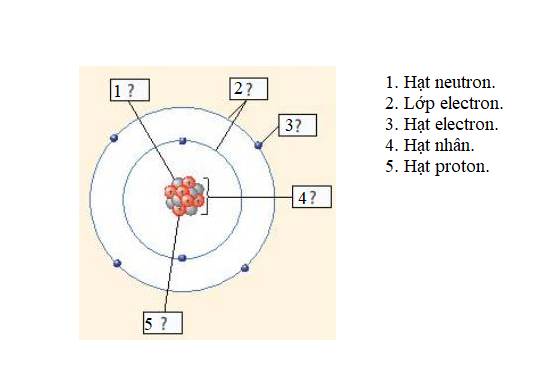



a: X có 10electron và có 2 lớp electron
b: X là neon
c: Oxy, Nitơ,cacbon