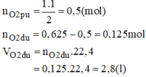Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(n_{O_2}=\dfrac{8}{22,4}=\dfrac{5}{14}\left(mol\right)\)
PTHH: 2H2 + O2 --to--> 2H2O
Xét tỉ lệ: \(\dfrac{0,5}{2}< \dfrac{\dfrac{5}{14}}{1}\) => H2 hết, O2 dư
PTHH: 2H2 + O2 --to--> 2H2O
0,5-->0,25
=> \(V_{O_2\left(dư\right)}=\left(\dfrac{5}{14}-0,25\right).22,4=2,4\left(l\right)\)

a, PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Ta có: \(n_{H_2}=n_{O_2}=\dfrac{6,1975}{24,79}=0,25\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,25}{2}< \dfrac{0,25}{1}\), ta được O2 dư.
Theo PT: \(n_{O_2\left(pư\right)}=\dfrac{1}{2}n_{H_2}=0,125\left(mol\right)\)
\(\Rightarrow n_{O_2\left(dư\right)}=0,25-0,125=0,125\left(mol\right)\)
\(\Rightarrow V_{O_2\left(dư\right)}=0,125.24,79=3,09875\left(l\right)\)
b, Theo PT: \(n_{H_2O}=n_{H_2}=0,25\left(mol\right)\)
\(\Rightarrow m_{H_2O}=0,25.18=4,5\left(g\right)\)
c, PT: \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
Theo PT: \(n_{KClO_3}=\dfrac{2}{3}n_{O_2}=\dfrac{1}{6}\left(mol\right)\)
\(\Rightarrow m_{KClO_3}=\dfrac{1}{6}.122,5\approx20,42\left(g\right)\)

\(n_{Zn}=\dfrac{13}{65}=0.2\left(mol\right)\)
\(n_{O_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(2Zn+O_2\underrightarrow{^{^{t^0}}}2ZnO\)
LTL : \(\dfrac{0.2}{2}< \dfrac{0.4}{1}\Rightarrow O_2dư\)
\(m_{O_2\left(dư\right)}=\left(0.4-0.1\right)\cdot32=9.6\left(g\right)\)
\(m_{ZnO}=0.2\cdot81=16.2\left(g\right)\)

n H2 (đktc) = 11,2 : 22,4 = 0,5 (mol)
n O2 (đktc) = 8 : 22,4 = 5/14 (mol)
PTHH: 2H2 + O2 ---> 2H2O
Mol ban đầu 0,5 5/14
Mol phản ứng 0.5 0,25 0,5
Mol sau phản ứng 0 3/28 0,5
a) sau phản ứng chất dư là O2
VO2 (đktc) = 3/28 . 22,4 = 73,472 (lít)
b) m h2o = 0,5 . 18 = 9 (g)

\(a,n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\\ n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
b, LTL: \(\dfrac{0,4}{4}>\dfrac{0,6}{3}\) => O2 dư
Theo pthh: \(\left\{{}\begin{matrix}n_{O_2\left(pư\right)}=\dfrac{3}{4}n_{Al}=\dfrac{3}{4}.0,4=0,3\left(mol\right)\\n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=\dfrac{1}{2}.0,4=0,2\left(mol\right)\end{matrix}\right.\)
=> VO2 (dư) = (0,6 - 0,3).22,4 = 6,72 (l)
c, mAl2O3 = 0,2.102 = 20,4 (g)
\(n_{Al}=\dfrac{10,8}{27}=0,4mol\)
\(n_{O_2}=\dfrac{13,44}{22,4}=0,6mol\)
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
Xét: \(\dfrac{0,4}{4}\) < \(\dfrac{0,6}{3}\) ( mol )
0,4 0,3 0,2 ( mol )
Chất dư là O2
\(m_{O_2\left(dư\right)}=\left(0,6-0,3\right).32=9,6g\)
\(m_{Al_2O_3}=0,2.102=20,4g\)