Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Giả sử tại anot chỉ có
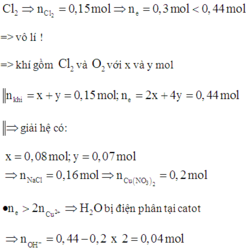
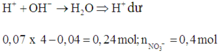
Xét Fe+ dung dịch sau điện phân: do thu được rắn =>Fe dư => Fe chỉ lên số oxi hóa +2
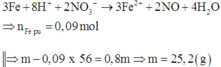

Chọn đáp án A.
Phương trình điện phân:
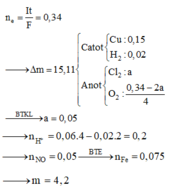
Catot: Cu2+ + 2e → Cu
2H2O + 2e → H2 + 2OH-
Anot: 2Cl- → Cl2 + 2e
2H2O → 4H+ + O2 + 4e
Fe + dung dịch sau điện phân → NO
=> Chứng tỏ dung dịch chứa H+, ở anot đã xảy ra điện phân nước.
![]()
=> Chứng tỏ Cu2+ chưa bị điện phân hết


Đáp án B
nNaCl = 0,48.0,5 = 0,24 (mol)
Trong thời gian t giây:
nKhí anot = 0,135 (mol) bao gồm nCl2 = 0,12 (mol) => nO2 = 0,135 – 0,12 = 0,015 (mol)
=> ∑ ne (trao đổi) = 2nCl2 + 4nO2 = 2.0,12 + 0,015.4 = 0,3 (mol)
Trong thời gian 2t giây thì ne = 0,3.2 = 0,6 (mol) ; nKhí thoát ra = 8,4/22,4 = 0,375 (mol)
+ Anot: nCl2 = 0,12 => nO2 = (0,6 – 0,12.2)/4 = 0,09 (mol)
+ Catot: nH2 = 0,375 – nCl2 – nO2 = 0,375 – 0,12 – 0,09 = 0,165 (mol)
Vì catot có H2 thoát ra nên M2+ điện phân hết
Catot Anot
M2+ +2e → M 2Cl- → Cl2 + 2e
(0,6 – 0,33)→0,135 (mol) 0,12 → 0,24 (mol)
2H2O + 2e → H2 + 2OH- 2H2O → O2 + 4H+ + 4e
0,33← 0,165 (mol) 0,09 ←(0,6 – 0,24) (mol)
Mtinh thể = 32,67/0,135 = 242 (g/mol)
=> M + 124 + 18n = 242
=> M + 18n = 118
=> n = 3 ; M =64 (Cu) thỏa mãn
Tại thời gian t giây Cu2+ đã bị điện phân hết
=> m = mCu = 0,135.64 = 8,64 (g)

Đáp án C
ne = 0,15 mol
dd X sau điện phân tác dụng với Fe tạo khí NO nên X phải chứa H+ nên
Tại A(+) : có 2Cl- → Cl2 + 2e
2H2O → 4H+ + 4e + O2
Tại K (-) thì : Cu2+ + 2e → Cu
Dd sau phản ứng đem cho Fe vào thì :
3Fe + 8H+ + 2NO3- → 3Fe2+ + 2NO + 4H2O
0,09 mol ← 0,0225 mol
Nếu Cu không có trong dd thì khối lượng rắn còn lại sau phản ứng là 0,125.56-0,0225.3:2.56 =5,11 < 5,43
→Cu còn trong dd và xảy ra phản ứng
Cu2+ + Fe → Cu + Fe2+
→ mrắn = 0,125.56 – 0,0225.3 : 2.56 + 8nCu2+(X) → nCu2+(X) = 0,04 mol
Vì Cu2+ còn dư trong X nên phản ứng tại (K) chỉ có Cu2+ với lượng phản ứng là 0,15 :2 =0,075 mol
Bảo toàn Cu có x = 0,075 + 0,04 =0,115 mol
Tại (A) thì ne = nCl + nH+ → 0,15 = nCl + 0,09 → nCl = 0,06 mol
Bảo toàn Cl có y =0,06 mol
→ x : y =0,115 : 0,06 =1,917

Đáp án C
ne = 0,15 mol
dd X sau điện phân tác dụng với Fe tạo khí NO nên X phải chứa H+ nên
Tại A(+) : có 2Cl- → Cl2 + 2e
2H2O → 4H+ + 4e + O2
Tại K (-) thì : Cu2+ + 2e → Cu
Dd sau phản ứng đem cho Fe vào thì : 3Fe + 8H+ + 2NO3- → 3Fe2+ + 2NO + 4H2O
0,09 mol ← 0,0225 mol
Nếu Cu không có trong dd thì khối lượng rắn còn lại sau phản ứng là 0,125.56-0,0225.3:2.56 =5,11 < 5,43
→Cu còn trong dd và xảy ra phản ứng Cu2+ + Fe → Cu + Fe2+
→ mrắn = 0,125.56 – 0,0225.3 : 2.56 + 8nCu2+(X) → nCu2+(X) = 0,04 mol
Vì Cu2+ còn dư trong X nên phản ứng tại (K) chỉ có Cu2+ với lượng phản ứng là 0,15 :2 =0,075 mol
Bảo toàn Cu có x = 0,075 + 0,04 =0,115 mol
Tại (A) thì ne = nCl + nH+ → 0,15 = nCl + 0,09 → nCl = 0,06 mol
Bảo toàn Cl có y =0,06 mol
→ x : y =0,115 : 0,06 =1,917

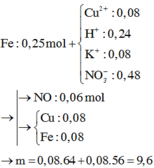



Chọn đáp án B