Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

+ 1 mol Cu phẳn ứng với 2 mol Ag ----> tăng 152 gam
--x mol ----------------------2x mol---------------9,42 gam
----> nCu = 0,062 mol ; nAg = 0,124 mol
---> n = 0,062 mol ; n = 0,026 mol
----> C_M Cu(NO3) 2 = 0,124 M ; C_M AgNO3 = 0,052 M

PTHH:
\(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\)
mKL tăng : \(mAg-mCu=29,12-20=9,12g\)
=>\(nCu=\dfrac{9,12}{108.2-64}=0,06mol\)
\(nAgNO_3=0,3.0,5=0,15mol\)
tỉ lệ so sánh :
\(\dfrac{nAgNO_3}{2}>\dfrac{nCu}{1}\left(0,075>0,06\right)\Leftrightarrow nAgNO_{3\left(dư\right)}=0,15-0,06.2=0,03mol\)
thep pt: \(nCu\left(NO_3\right)_2=nCu=0,06mol\)
\(\Leftrightarrow C_{MCu\left(NO_3\right)_2}=\dfrac{0,06}{0,5}=0,12M\)
\(C_{MAgNO_{3\left(dư\right)}}=\dfrac{0,03}{0,5}=0,06M\)
vậy nồng độ mol chất Cu(NO3)2 và AgNO3(dư) lần lượt là 0,12M và 0,06M

a) m rắn=4,08 gam
b) CM Cu(NO3)2 dư=0,35M; CM Fe(NO3)2=0,2M
c) V NO2=1,792 lít
Giải thích các bước giải:
Ta có: nAgNO3=0,2.0,1=0,02 mol; nCu(NO3)2=0,5.0,2=0,1 mol; nFe=2,24/56=0,04 mol
Fe + 2AgNO3 -> Fe(NO3)2 + 2Ag
Vì nAgNO3=0,02 mol; nFe =0,04 -> Fe dư -> tạo ra 0,02 mol Ag và Fe phản ứng 0,01 mol -> dư 0,03 mol
Fe + Cu(NO3)2 -> Fe(NO3)2 + Cu
Vì Cu(NO3)2=0,1 mol; nFe =0,03 mol -> Cu(NO3)2 dư =0,07 mol ; nCu=0,03 mol
Rắn thu được gồm Ag 0,02 mol và Cu 0,03 mol -> m rắn=4,08 gam
Dung dịch sau phản ứng chứa Cu(NO3)2 dư 0,07 mol và Fe(NO3)2 0,04 mol (Bảo toàn Fe)
-> CM Cu(NO3)2=0,07/0,2=0,35M; CM Fe(NO3)2=0,04/0,2=0,2M
Hòa tan rắn bằng HNO3 đặc
Ag + 2HNO3 -> AgNO3 + NO2 + H2O
Cu + 4HNO3 -> Cu(NO3)2 +2NO2 + 2H2O
-> nNO2=nAg + 2nCu=0,02+0,03.2=0,08 mol -> V NO2=0,08.22,4=1,792 lít

nAgNO3 = 0,3 . 0,5 = 0,15 mol
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag↓
1_______2_______1_________2 tăng 2 . 108 - 1.64 = 152g
x _____2x________x________ 2x tăng 29,12 - 20 = 9,12(g)
\(x=\frac{9,12}{152}=0,06\left(mol\right)\)
nAgNO3 p.ứ = 0,12 mol
Sau p.ứ trong dd có: Cu(NO3)2: 0,06 mol
AgNO3 dư: 0,15 - 0,12 = 0,03 mol
\(CM_{Cu\left(NO3\right)2}=\frac{0,06}{0,5}=0,12\left(M\right)\)
\(CM_{AgNO3}=\frac{0,03}{0,5}=0,06\left(M\right)\)
b) Sau phản ứng trong dung dịch chỉ chứa 1 muối tan nên Cu(NO3)2 và AgNO3 đều phản ứng hết
Gọi NTK của R là M
M + 2AgNO3 → M(NO3)2 + 2Ag↓
1_____2 __________________2 tăng 2 . 108 - 1.R = (216-M)g
_______ 0,03 _____________tăng \(\frac{0,03.\left(216-M\right)}{2}\left(g\right)\)
M + Cu(NO3)2 → M(NO3)2 + Cu↓
1____1___________________1 tăng (64 - M) (g)
___0,06_________________tăng 0,06.(64-M)(g)
Suy ra: 32,205 - 30 =\(\frac{0,03.\left(216-M\right)}{2}\text{+ 0,06.(64-M)}\)
→ 0,015(216-M)+0,06(64-M)= 2,205
→ M = 65
→ R là Kẽm (Zn)

\(n_{Na_2CO_3}=\dfrac{360.21,2\%}{100\%.106}=0,72(mol)\\ n_{H_2SO_4}=2,5.0,2=0,5(mol)\\ PTHH:Na_2CO_3+H_2SO_4\to Na_2SO_4+H_2O+CO_2\uparrow\\ a,\text {Vì }\dfrac{n_{Na_2CO_3}}{1}>\dfrac{n_{H_2SO_4}}{1} \text {nên }Na_2CO_3\text { dư}\\ \Rightarrow n_{CO_2}=n_{H_2SO_4}=0,5(mol)\\ \Rightarrow V_{CO_2}=0,5.22,4=11,2(l)\\\)
\(b,A:Na_2SO_4\\ n_{Na_2SO_4}=n_{H_2SO_4}=0,5(mol)\\ m_{dd_{H_2SO_4}}=200.1,1=220(g);V_{dd_{Na_2CO_3}}=\dfrac{360}{1,2}=300(ml)=0,3(l)\\ \Rightarrow C\%_{Na_2SO_4}=\dfrac{0,5.142}{360+200-0,5.44}.100\%=13,2\%\\ C_{M_{Na_2SO_4}}=\dfrac{0,5}{0,3+0,2}=1M\)

Giải thích: Đáp án D
nZn =0,052 > nAgNO3 → dd Z chỉ chứa Zn(NO3)2
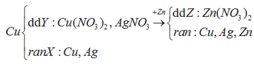
Bảo toàn số mol NO3 thì nZn(NO3)2(Z) =0,02 mol→ rắn T có mZn = 2,925-0,02.65=1,625g
Trong rắn T đặt nCu =x, nAg =y → 64x + 108y=3,217-1,625 = 1,592(g)
Bảo toàn điện tích trong dd Y có 2x + y =0,04 → x =0,018 mol y =0,004 mol
Bảo toàn khối lượng Cu và Ag trong phản ứng td với AgNO3 có
m + 0,04.108=mCu(Y) +mAg(Y) +3,88 → m =0,018.64+0,004.108+3,88-0,04.108=1,152 (g)

a, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có: \(n_{Fe}=\dfrac{14}{56}=0,25\left(mol\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{HCl}=2n_{Fe}=0,5\left(mol\right)\\n_{H_2}=n_{Fe}=0,25\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow V_{H_2}=0,25.24,79=6,1975\left(l\right)\)
\(a=C_{M_{HCl}}=\dfrac{0,5}{0,1}=5\left(M\right)\)
b, Theo PT: \(n_{FeCl_2}=n_{Fe}=0,25\left(mol\right)\)
Ta có: \(n_{AgNO_3}=0,4.1,3=0,52\left(mol\right)\)
PT: \(2AgNO_3+FeCl_2\rightarrow Fe\left(NO_3\right)_2+2AgCl_{\downarrow}\)
______0,5______0,25______0,25________0,5 (mol)
\(AgNO_3+Fe\left(NO_3\right)_2\rightarrow Fe\left(NO_3\right)_3+Ag_{\downarrow}\)
0,02______0,02________0,02________0,02 (mol)
⇒ m = mAgCl + mAg = 0,5.143,5 + 0,02.108 = 73,91 (g)
- Dd sau pư gồm: Fe(NO3)3: 0,02 (mol) và Fe(NO3)2: 0,25 - 0,02 = 0,23 (mol)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{Fe\left(NO_3\right)_3}}=\dfrac{0,02}{0,1+0,4}=0,04\left(M\right)\\C_{M_{Fe\left(NO_3\right)_2}}=\dfrac{0,23}{0,1+0,4}=0,46\left(M\right)\end{matrix}\right.\)
\(Fe+2HCl->FeCl_2+H_2\\ a.V=\dfrac{14}{56}\cdot22,4=5,6\left(L\right)\\ a=\dfrac{\dfrac{14}{56}\cdot2}{0,1}=5\left(M\right)\\ b.n_{AgNO_3}=0,4\cdot1,3=0,52mol\\ FeCl_2+AgNO_3->Fe\left(NO_3\right)_2+AgCl\\ Fe\left(NO_3\right)_2+AgNO_3->Ag+Fe\left(NO_3\right)_3\\ m=0,25\cdot143,5+0,25\cdot108=62,875\left(g\right)\\ C_{M\left(AgNO_3\right)}=\dfrac{0,02}{0,5}=0,04M\\ C_{M\left(Fe\left(NO_3\right)_3\right)}=\dfrac{0,25}{0,5}=0,5M\)

Mg à?
sai đấy bỏ đi