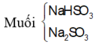Bài 7: Hòa tan hết 12,4 gam Na2O vào nước, thu được 200 gam dung dịch X. a) Tính nồng độ phần trăm của dung dịch X. b) Hấp thụ toàn bộ V lít khí SO2 (ở 25oC và 1 bar) vào lượng dung dịch X ở trên, thu được dung dịch Y chỉ chứa muối trung hòa. - Tính giá trị của V. - Tính nồng độ phần trăm của dung dịch Y.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có: \(n_{SO_2}=\dfrac{12,395}{24,79}=0,5\left(mol\right)\)
BTNT S, có: nH2SO4 = nSO3 = nSO2 = 0,5 (mol)
Mà: mH2SO4 (ban đầu) = 210.10% = 21 (g)
⇒ mH2SO4 (trong X) = 21 + 0,5.98 = 70 (g)
Có: m dd X = 210 + mSO3 = 210 + 0,5.80 = 250 (g)
\(\Rightarrow C\%_{H_2SO_4}=\dfrac{70}{250}.100\%=28\%\)

Tham khảo
nCaCO3 = 0,5265 mol
mà H = 95% => nCO2 = 0,5 mol
nNaOH = 0,5.1,8= 0,9 mol
ta có nNaOH/nCO2 =1,8 => 2 muối
CaCO3 => CaO + CO2
CO2 + 2NaOH => Na2CO3 + H2O
x------->2x
CO2+ NaOH=> NaHCO3
y------->y
giải hệ x + y = 0,5
2x + y =0,9
=> x= 0,4;y= 0,1
=> mNa2CO3 = 0,4.106 = 42,4 (g)
mNaHCO3 = 0,1.84 = 8,4
\(n_{NaOH}=0,2.0,3=0,06\left(mol\right)\\ n_{CaCO_3}=\dfrac{4}{100}=0,04\left(mol\right)\\ CaCO_3\rightarrow\left(t^o\right)CaO+CO_2\uparrow\\ n_{CO_2}=n_{CaCO_3}=0,04\left(mol\right)\\ Vì:\dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{0,06}{0,04}=1,5\\ \Rightarrow P.ứ.cho.2.muối.với.số.mol.bằng.nhau\\ CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\\ CO_2+NaOH\rightarrow NaHCO_3\\ Đặt:n_{NaHCO_3}=n_{Na_2CO_3}=a\left(mol\right)\\ n_{CO_2}=0,04\Leftrightarrow a+a=0,04\\ \Leftrightarrow a=0,02\left(mol\right)\\ \Rightarrow m_{ctan}=m_{Na_2CO_3}+m_{NaHCO_3}=106.0,02+84.0,02=3,8\left(g\right)\)

a)
Do A và B đều là kim loại hóa trị II nên ta sử dụng phương pháp trung bình coi A và B là một chất gọi là X
=> CT chung của 2 muối là XCO3
Ta có nCO2 = \(\dfrac{1,12}{22,4}\) = 0,05 ( mol )
XCO3 + H2SO4 → XSO4 + H2O + CO2
0,05 <---- 0,05 <---0,05 <-- 0,05 < -0,05
bảo toàn khối lượng ta có
mXSO4 = mXCO3 + mH2SO4 - mH2O - mCO2
= 4,68 + ( 98 . 0,05 ) - ( 18 . 0,05 ) - ( 44 . 0,05 )
= 6,48 ( gam )
b) MXCO3 = mXCO3 : nXCO3 = 4,68 : 0,05 = 93,6
=> X = 93,6 - 12 - 16 . 3 = 33,6
có nACO3 : nBCO3 = 2 : 3
và nACO3 + nBCO3 = 0,05
=> nACO3 = 0,02 và nBCO3 = 0,03
=> nA = 0,02 và nB = 0,03
=> ( 0,02 . A + 5 : 3 . 0,03 . B) / 0,05 = 33,6
=> A = 24 ( là magie - Mg ) do B = A . 5 :3
=> B = 40 ( là canxi - Ca )
=> mMgCO3 = 1,68 ( gam )
=> %mMgCO3 = \(\dfrac{1,68}{4,68}\) . 100 \(\approx\) 36 %
=> %mCaCO3 = 100 - 36 = 64%

Qui đổi hỗn hợp về x mol Na ; y mol Ba và z mol
O, ta có: Na + H2O → NaOH + 0,5H2
Ca + H2O → Ca(OH)2 + H2
O + H2 → H2O
=> mX = 23x + 40y + 16z = 5,13 g nH2 = 0,5x + y –z = 0,025 mol
n NaOH = n Na = x = 0,07 mol
=>y=0,06 mol ; z=0,07 mol
=>n OH- = n NaOH + 2 nCa(OH)2 = 0,19 mol
=> Có n OH >2 n SO2
=> tạo muối trung hòa, OH dư
=>m CaSO3 = 0,06.120 = 7,2 g
=>C